Dr. Bánhegyi Róbert János Ph.D.
A rák- és cukorbetegség metabolikus és molekuláris összefüggései.
Első írásomban az onkodiabetológiával mint új orvosi tudományággal és szemléletmóddal szeretném az érdeklődő szakmai közönséget megismertetni.
Elnevezéséből kiindulva talán nem meglepő, hogy ezen határterületi diszciplína létrejötte szervesen illeszkedik az onkológia és a diabetológia évezredes történetéhez, melyen belül az utóbbi évszázad tudományos eredményei és epidemiológiai változásai napjainkban együttesen vezettek el az onkodiabetológia megszületéséhez. Eredete elsődlegesen az 1920-as évek jórészt Nobel-díjjal elismert kutatóihoz köthető, akik 1921-ben az inzulint, 1922-ben a metformint fedezték fel, majd 1924-ben Otto Heinrich Warburg német biokémikusnak a ráksejtek anyagcseréjéről alkotott elmélete indított el lassú, de mélyreható változásokat az onkológia és a diabetológia kapcsolatában.

Otto Heinrich Warburg (1883-1970)
Warburg elsőként tett különbséget az egészséges és a daganatos sejtek anyagcseréje között. Kimondta, hogy a ráksejtek energiatermelése túlnyomórészt a glükóz anaerob vagy oxigénhiányos lebontásából származik, amely ezáltal kevésbé hatékony, mint az egészséges sejtekben domináló, aerob vagy oxidatív glikolízisen alapuló energianyerési mechanizmus. Később szintén Warburg fedezte fel, hogy a NAD (nikotin-adenin-dinukleotid) a sejtek oxidációs-redukciós folyamataiban központi szerepet játszik. Ehhez kapcsolódóan ma már azt is tudjuk, hogy a NADPH (NAD-foszfát dehidrogenáz) és a NOX (NADPH-oxidáz) az oxidatív stressz állapot létrejöttében, ezáltal a tumorpromócióban megkerülhetetlen tényező. A reaktív oxigén-származékok (ROS) koncentrációtól függően befolyásolják az onkogenezist; elősegítik a ráksejtek transzformációját és proliferációját vagy apoptózist idéznek elő. Mivel a túlságosan magas ROS-koncentráció magukat a tumorsejteket is apoptózisba taszítaná, így azok a saját túlélésük érdekében fokozzák a NADPH-termelést és a több lépcsőben bekapcsolódó antioxidáns transzkripciós faktorok (NRF2, FoxO1, PGC-1α, AP-1 stb.) aktiválását. Mindezek hatására magasabb ROS-szintek mellett is lehetséges a ráksejtek túlélése. Warburg az elméletének helyességét saját életében nem tudta egyértelműen alátámasztani, s azt végül 2006-ban szintén német kutatóknak sikerült bizonyítani. 1931-ben a Nobel-díjat sem ezért, hanem a citokrómok felfedezéséért és a sejtlégzés folyamatainak leírásáért kapta.
A II. világháborút követően, a társadalmi jólét és az elhízás terjedésével együtt, a 2-es típusú diabetes és a rosszindulatú daganatok szinkron térnyerése egyre nyilvánvalóbbá vált, s köztük mind több epidemiológiai, metabolikus és molekuláris genetikai összefüggés igazolódott. Emellett a Human Genom Projekt 2006-ban történt lezárása, majd a génasszociációs vizsgálatok elterjedése is számtalan új információval szolgált a két népbetegség kapcsolatára vonatkozóan. Ezen változásokhoz adódott még az elmúlt két évtizedben a rákbetegség és a diabetes kezelésének ugrásszerű fejlődése, új hatóanyagok százainak bevezetése a rák- és cukorbetegek ellátásában. Végül a ma már világszerte elterjedten alkalmazott modern antineoplasztikus és antidiabetikus terápiákkal összefüggő és rohamosan bővülő tudásanyag vezetett el az új tudományág megszületéséhez.
Az onkodiabetológia elsősorban a rákbetegség és a szénhidrát-anyagcsere zavarok közötti különböző összefüggéseket igyekszik feltárni és az új ismereteket az érintett betegcsoportok gyógyításában hasznosítani. Klinikai gyakorlati fókuszában jelenleg a daganatellenes gyógyszerek diabetogén effektusainak, valamint az antidiabetikus kezelések onkoterápiát és tumorképződést befolyásoló hatásainak összehangolt menedzselése áll. Fő feladata a rákbetegeken jelentkező diabetes és glikémiás eltérések, valamint a szénhidrát-anyagcsere zavaraiban szenvedőknél kialakuló rosszindulatú daganatok megelőzése, felismerése, optimális kezelése, melynek céljából igyekszik elősegíteni az elméleti háttér kutatását és a megfelelő klinikai gyakorlat kidolgozását.
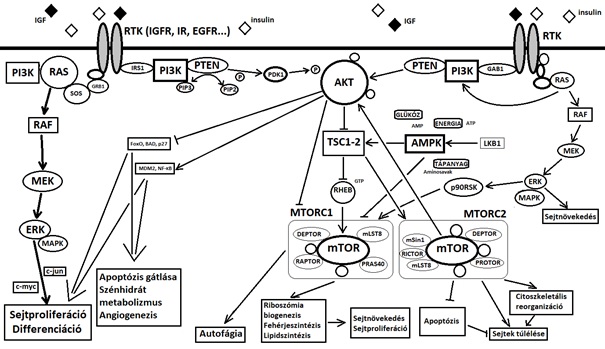
Epidemiológiai, preklinikai és klinikai vizsgálatok alapján ma már ismert, hogy a cukorbetegség számos daganat képződésében önálló rizikótényezőként szerepelhet, sőt a tumorkockázat növekedése akár már prediabetes esetén jelentkezhet. A két kórkép közti kapcsolat fordított irányban is működik. A malignus tumorok a gazdaszervezetben olyan metabolikus és molekuláris genetikai változásokat idéznek elő, amelyek inzulinrezisztens állapotot eredményezhetnek. A daganat által generált inzulinrezisztencia akár szekunder cukorbetegség kialakulásához is elvezethet, amit az antineoplasztikus terápiák esetleges diabetogén effektusa tovább súlyosbíthat. A rákbetegség és a 2-es típusú diabetes molekuláris kapcsolatát vizsgáló kutatások egy része az utóbbi években a figyelmet a RAS (patkányszarkóma virális onkogén homológ) és a PI3K (foszfatidil-inozitol-3-kináz) jelátviteli utak közös szerepére irányította. Ezek megváltozott működése a sejtciklust, a sejt metabolizmusát, növekedését és proliferációját, vagyis a túlélését jelentősen befolyásolja, azokat részben az inzulinrezisztencia, részben a tumorpromóció és -progresszió felé tolja. Emiatt a molekuláris ok-okozati viszonyok aligha érthetők meg az IGF (inzulinszerű növekedési faktor) -receptorok, valamint a RAS és a PI3K jelátviteli utak működésének és kapcsolódási pontjainak megismerése nélkül [1. ábra].
1. ábra | RAS- és PI3K-útvonalak viszonya. Molekuláris kapcsolat a malignus daganatok és a 2-es típusú diabetes mellitus kialakulásában
Az onkodiabetológia elméleti hátteréről, a rák- és cukorbetegség közti epidemiológiai, metabolikus és molekuláris genetikai összefüggésekről 2022-ben az Orvosi Hetilapban írtam részletesen.
(Rövidítések és referenciák a következő közleményben.)

















